Señalan que el estudio PURPOSE 1, mostró más del 99% de eficacia en mujeres jóvenes en África subsahariana.
La empresa biofarmacéutica Gilead Sciences anunció que la FDA (Food and Drug Administration) aprobó “Yeztugo” (lenacapavir), el primer y único tratamiento profiláctico contra el VIH que se administra solo dos veces al año, ofreciendo seis meses de protección continua.
El respaldo de la FDA se basó en los resultados del estudio PURPOSE 1, donde el fármaco, denominado “Yeztugo”, demostró una eficacia superior al 99 % en la prevención de infecciones entre mujeres jóvenes en África subsahariana, una de las poblaciones más vulnerables.

El CEO de Gilead, Daniel O´Day, declaró que este es un día histórico en la larga lucha contra el VIH. Yeztugo podría transformar la prevención y acercarnos a acabar con esta epidemia.
El tratamiento se administra como dos inyecciones subcutáneas en el abdomen, que forman un depósito liberado lentamente durante seis meses.
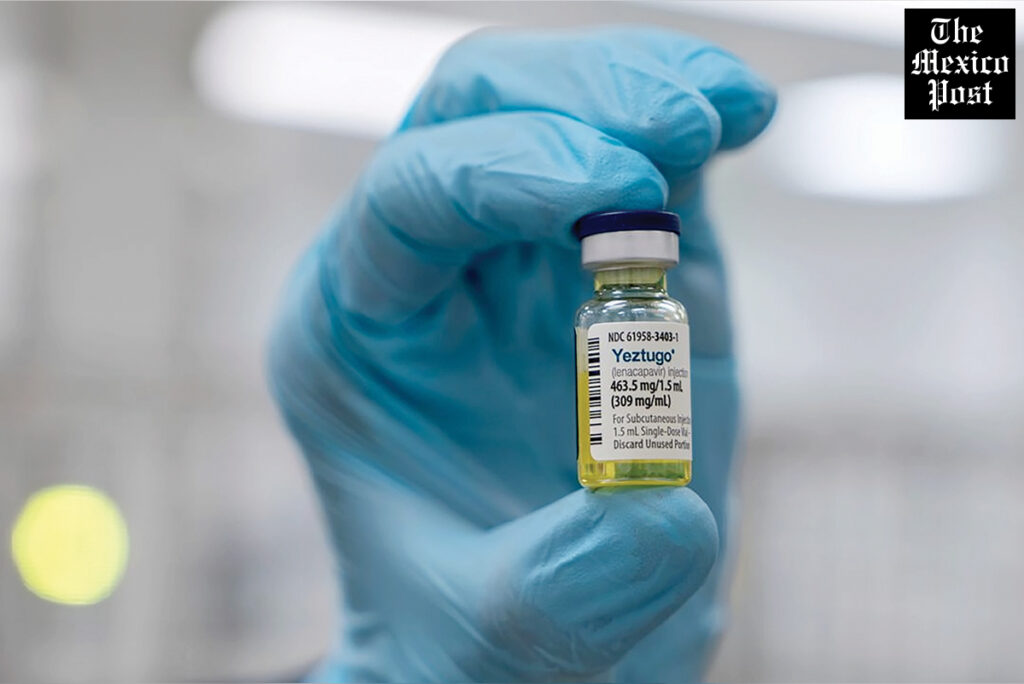
Se requieren pruebas de VIH negativas antes de cada dosis. Gilead estableció el precio en Estados Unidos en 28,218 dólares anuales, anticipando que la mayoría de los seguros cubrirán el tratamiento; también ofrece programas de asistencia financiera.
A nivel global, Gilead firmó licencias sin regalías con seis fabricantes genéricos, para cubrir 120 países de ingresos bajos, con un compromiso de distribuir dosis gratuitas a dos millones de personas durante los próximos años.